リベルワークスは、医療機器ソフトウェア開発のパイオニアとして、企画・開発から承認取得、販売に至るまで、製品化を実現するためのさまざまな課題に対応する多彩なソリューションを提供いたします。 医療機器の開発・製品化に不可欠な、国際規格(IEC 62304、ISO 14971、IEC 62366-1、IEC 81001-5-1)への適合支援をはじめ、PMDAへの承認申請、第三者認証機関への認証申請支援、そして販売支援に至るまで、製品化を推進するための課題を共に解決いたします。
私たちの支援サービス
リベルワークスは、医療機器の開発から市場導入までを一貫してサポートいたします。豊富な実績、専門的な知識と実務経験を活かし、以下の支援を提供しております。
QMS(品質マネジメントシステム)構築支援
医療機器製造・販売に不可欠なQMS(ISO 13485等)の構築から運用までを支援いたします。体制整備、文書作成、内部監査対応など、実務的な支援が可能です。
製造業・製造販売業・修理業・販売業などの業許可取得支援
厚生労働省や各自治体への申請に必要な書類作成から、実地調査対応まで幅広くサポートいたします。
医療機器規格要求事項への適合支援
JIS T 2304(IEC 62304)、JIS T 62366、JIS T 14971など、各種規格への適合に向けた設計・開発支援を実施。ギャップ分析から設計文書作成まで対応いたします。
PMDA相談支援(伴走型)
PMDAとの事前相談、対面助言の際の資料作成および出席同行まで、実務レベルでの支援が可能です。経験豊富なスタッフが「伝えるべきポイント」と「聞かれるポイント」を整理してサポートします。
承認・認証申請支援
第三者認証機関やPMDAへの提出書類(STED、CTD等)の作成・レビュー支援。適合性調査、照会対応など、申請プロセスの全体をカバーします。"
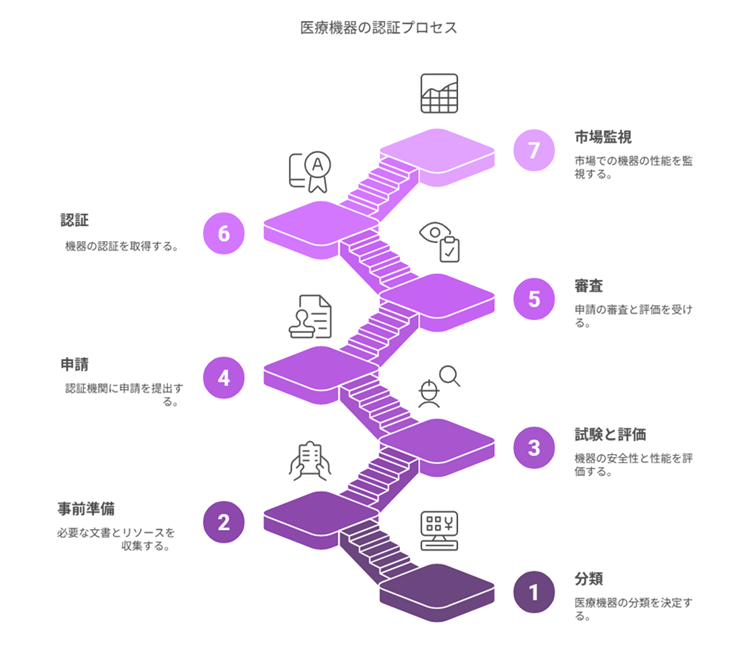
医療機器の認証・承認取得までの流れ
以下は、医療機器の企画段階から承認・認証取得、そして上市までの一般的な流れです。お客様の製品のステージに応じて、柔軟にサポートいたします。
1.製品企画・設計
医療機器分類の確認(クラス分類) 対象規格・規制の特定
2.QMS体制の整備、許可取得
ISO13485準拠の文書整備、運用開始 製造業・製販業等の業許可取得
3.設計・開発・検証
安全性・有効性に関する試験の計画・実施 リスクマネジメント、JIS規格やユーザビリティエンジニアリング対応
4.PMDA相談・事前確認
対面助言申込み・資料作成・相談同席 照会事項への対応支援
5.申請書類の作成・提出
STED/CTD等の技術文書の作成 第三者認証機関やPMDAへの提出・フォローアップ
6.認証・承認取得後の支援
市販後調査、安全管理、変更管理等の支援"
最後に
これまでに医療機器メーカーをはじめ、製薬会社、スタートアップ企業、異業種参入企業など医療関連の企業を支援してきた豊富な実績があり、製品化に向けた最適なソリューションの提供が可能です。 医療機器認証で以下のようなお困りごとがありましたら、お気軽にご相談ください。
- 医療機器認証は初めて
- 医療機器ソフトウェアの開発プロセスがわからない
- 必要な規格や認証取得が複雑で、具体的に何の作業を行えばいいかわからない
- 規格適合やQMS構築に不安がある
- 製造・販売業の許可取得に悩んでいる
- 初めてPMDAと向き合う
- 気軽に相談したい
- どこまで支援してもらえるのか
